小鼠小肠类器官培养体系的优化:高/低出芽培养基的应用与选择策略
类器官培养技术已成为研究肠道生物学、疾病机制和药物筛选的重要工具。不同实验目的(如干细胞扩增、分化研究或疾病建模)对类器官的生长特性需求各异。针对这一需求,科研界开发了两种功能互补的小鼠小肠类器官培养基——高出芽型培养基和低出芽型培养基,分别优化了干细胞的快速扩增或分化状态的精准维持,使研究者能够更灵活地匹配实验目标。
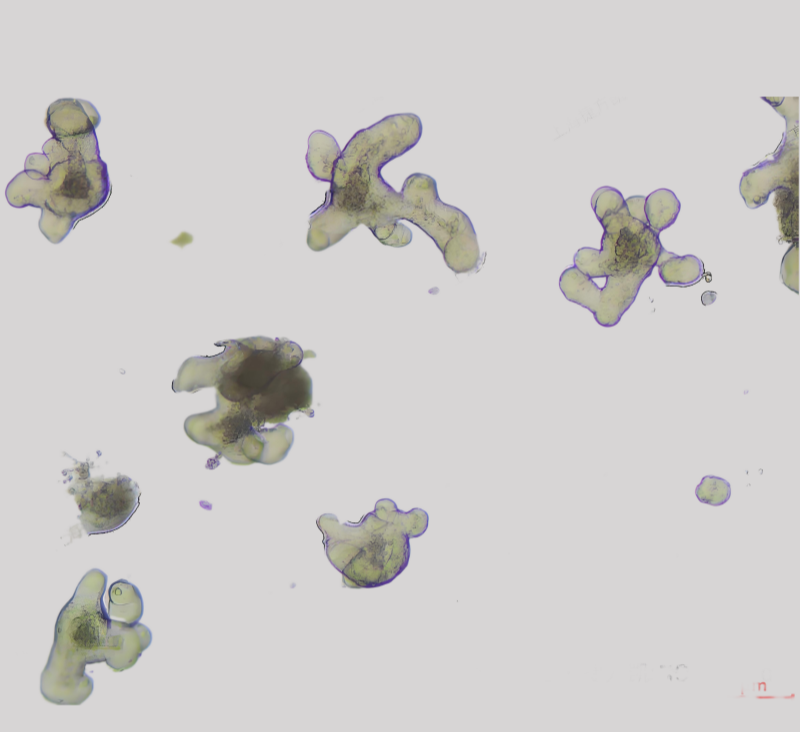
1. 高出芽小鼠小肠类器官培养基:高效干细胞激活与快速扩增
核心特点
强力促进隐窝干细胞增殖:通过优化生长因子组合(如增强Wnt、R-spondin等信号),显著提升干细胞的自我更新能力,使类器官出芽率提高50%以上。
缩短培养周期:在3~5天内即可形成典型出芽结构,相比传统培养基效率提升30%~50%,适用于高通量实验需求。
适用于快速扩增需求:特别适合需要大量类器官的实验,如CRISPR筛选、药物毒性测试或急性损伤修复研究。
典型应用场景
✔ 药物筛选与毒性评估:快速生成大量类器官,用于抗肿瘤药物或抗生素的肠道毒性测试。
✔ 干细胞生物学研究:探究Wnt/β-catenin等信号通路在肠道干细胞维持中的作用。
✔ 急性疾病模型构建:如辐射损伤、感染性肠炎或缺血-再灌注损伤模型,需要快速获得实验样本。
培养表现
形态特征:类器官呈现典型“花蕾样”出芽结构,隐窝样区域显著增多。
增殖能力:传代后24~48小时即可观察到活跃的出芽,适合短期实验。
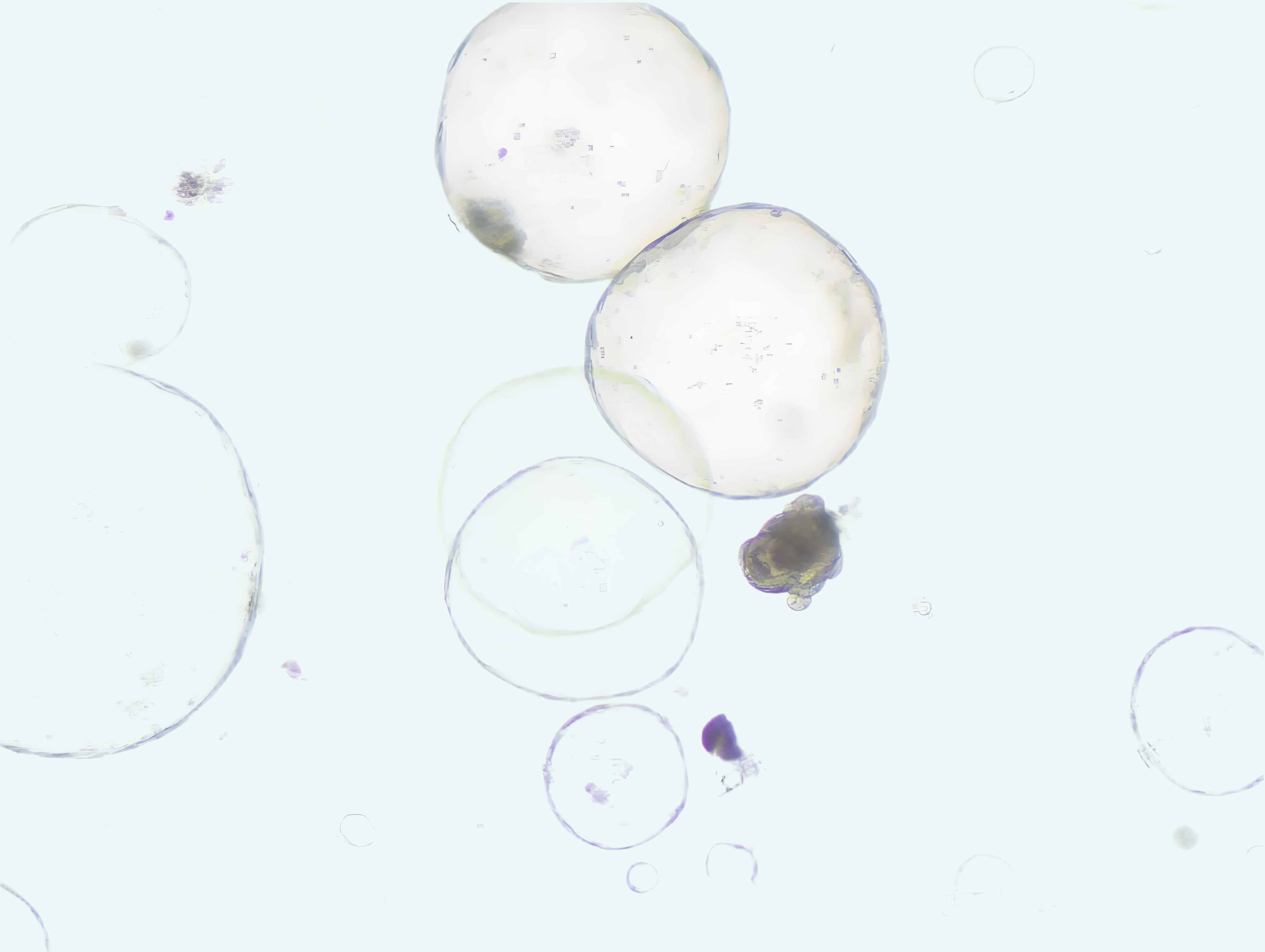
2. 低出芽小鼠小肠类器官培养基:稳态维持与分化研究
核心特点
精准调控分化状态:通过调整生长因子比例(如降低Wnt活性,优化EGF/Noggin等),抑制干细胞的过度增殖,促进杯状细胞、潘氏细胞和肠上皮细胞的成熟。
更接近体内生理状态:长期培养(>7天)仍能维持稳定的细胞组成,杯状细胞和潘氏细胞比例与真实肠道组织高度一致。
操作简便:无需额外添加分化诱导剂或抑制剂,减少实验变量,提高可重复性。
典型应用场景
✔ 肠道稳态与分化机制研究:探究Notch、BMP等通路如何调控肠上皮细胞命运决定。
✔ 慢性疾病建模:如炎症性肠病(IBD)、肠纤维化或肿瘤微环境研究,需要长期维持类器官的稳定状态。
✔ 宿主-微生物互作研究:与肠道菌群共培养时,维持上皮屏障功能和黏液分泌能力。
培养表现
形态特征:类器官结构更接近稳态肠道,出芽较少,但隐窝-绒毛样结构清晰。
长期稳定性:可维持培养超过2周仍保持良好分化状态,适合长期实验。
3. 如何选择适合的培养基?
| 研究需求 | 推荐培养基类型 | 关键优势 |
|---|---|---|
| 干细胞扩增、基因编辑 | 高出芽培养基 | 快速增殖,缩短实验周期 |
| 药物高通量筛选 | 高出芽培养基 | 高产量,适合短期检测 |
| 急性损伤/感染模型 | 高出芽培养基 | 快速响应,模拟再生过程 |
| 分化机制研究 | 低出芽培养基 | 维持杯状细胞、潘氏细胞比例 |
| 慢性疾病建模(IBD等) | 低出芽培养基 | 长期稳定,更接近体内状态 |
| 肠道屏障功能研究 | 低出芽培养基 | 支持黏液分泌和紧密连接形成 |
4. 实验优化建议
短期实验(<7天):优先选择高出芽培养基,以获得足够数量的类器官。
长期实验(>7天):使用低出芽培养基,避免干细胞过度增殖导致的异常分化。
组合使用策略:
先使用高出芽培养基快速扩增类器官,再换用低出芽培养基诱导分化。
适用于需要先扩增再分化的实验,如基因编辑后表型分析。
5. 结论
小鼠小肠类器官的培养策略应基于实验目标灵活调整:
高出芽培养基适用于需要快速干细胞扩增的研究,如药物筛选或急性模型。
低出芽培养基更适合长期分化研究、慢性疾病建模或肠道稳态分析。
通过合理选择培养基,研究者能够更精准地模拟肠道生理或病理状态,提高实验的可靠性和可重复性。未来,结合3D共培养、器官芯片等技术,这一体系有望在个性化医疗和转化研究中发挥更大作用。
产品推荐: