胃癌类器官培养基( JFKR-GC-100/ JFKR-GC-500)
胃癌类器官培养基(JFKR-GC-100/JFKR-GC-500)是一款专为胃癌类器官体外培养设计的培养基产品。该培养基经过优化,能够支持胃癌细胞的增殖、分化以及类器官的三维结构形成,适用于胃癌疾病研究、药物筛选、毒性测试及发病机制研究等领域。
胃癌类器官培养基(JFKR-GC-100/JFKR-GC-500)是一款专为胃癌类器官体外培养设计的培养基产品。该培养基经过优化,能够支持胃癌细胞的增殖、分化以及类器官的三维结构形成,适用于胃癌疾病研究、药物筛选、毒性测试及发病机制研究等领域。
1.产品概述
胃癌类器官培养基(JFKR-GC-100/JFKR-GC-500)是一款专为胃癌类器官体外培养设计的培养基产品。该培养基经过优化,能够支持胃癌细胞的增殖、分化以及类器官的三维结构形成,适用于胃癌疾病研究、药物筛选、毒性测试及发病机制研究等领域。
2.产品特点
高效培养:提供胃癌类器官生长所需的理想环境,支持高存活率和增殖能力。
稳定性强:培养基成分经过严格质量控制,确保批次间一致性和稳定性。
操作简便:培养基预配制,用户只需按照说明书操作即可直接使用。
广泛适用:适用于基础研究、药物开发、毒性测试及疾病模型构建等多种场景。
3.应用领域
胃癌疾病研究:用于模拟胃癌的病理过程,研究胃癌的发病机制。
药物筛选:评估药物对胃癌类器官的作用和毒性。
个体化医疗:用于患者特异性药物敏感性测试,指导临床治疗方案。
癌症生物学研究:研究胃癌细胞的增殖、侵袭和转移机制。
新药开发:用于抗胃癌药物的筛选和药效评估。
4.注意事项
使用前请仔细阅读说明书,确保正确配制和使用培养基。
避免污染,所有操作需在无菌条件下进行。
建议在有效期内使用,以确保最佳培养效果。
5.总结
胃癌类器官培养基(JFKR-GC-100/JFKR-GC-500)是一款高效、稳定的培养基产品,为胃癌类器官的培养和研究提供了可靠的工具。无论是基础研究还是临床应用,该培养基都能满足用户的需求,助力胃癌相关领域的科学探索和技术创新。
6.操作步骤
1、 样本前处理
实验材料:
原代缓冲液B(4℃预冷)、组织保存液E、组织运输箱、冰袋
(1) 取样以及组织样本运输是类器官构建成功的第一个环节也是最容易忽视的步骤,若样本前期保存不当会导致细胞活性差、污染、正常细胞少等问题,降低构建成功率。
(2) 新鲜的组织样本取出后,首先用原代缓冲液B清洗3-5次,将样本表面血液冲洗干净,放入组织保存液中4℃保存运输(72h 内)。
2、 类器官原代培养(以24孔板为例)
实验材料:
原代缓冲液B(4℃预冷)、原代组织消化液C(37℃)、基质胶(提前24h放入4℃冰箱融化)、肠癌类器官培养基A(室温或37℃)、镊子(10㎝)、尖头眼科手术剪、一次性60mm培养皿、1.5mL、15mL、50mL离心管、100㎛滤膜、3mL巴氏吸管/移液枪、24细胞培养板、金属冰盒
(1) 取材后的肠癌组织建议在 2 - 8℃条件下保存,快速转运至洁净实验室进行组织处理和干细胞分离,拍照并登记信息。
(2) 准备若干培养皿,加入 4℃预冷的原代缓冲液 B备用。
(3) 取样管消毒,将肠癌组织放入培养皿中,原代缓冲液 B 清洗三次后,去除杂质,眼科剪或手术刀将组织剪切成体积约为 1~3 mm3 的组织块。(建议放入1.5ml EP管剪碎组织)
(4) 剪碎后的组织块加入5ml原代组织消化液C 37℃震荡消化15-25 min(消化过程中随时观察组织消化情况)。
注:组织量太少或活检样本用 1ml 原代组织消化液 C 在 1.5ml EP 管内消化。
(5) 取少量消化液在显微镜下观察,镜下观察到较多的70μm以下的细胞簇或单个细胞后(图1-2),加入3倍体积原代缓冲液B终止消化。
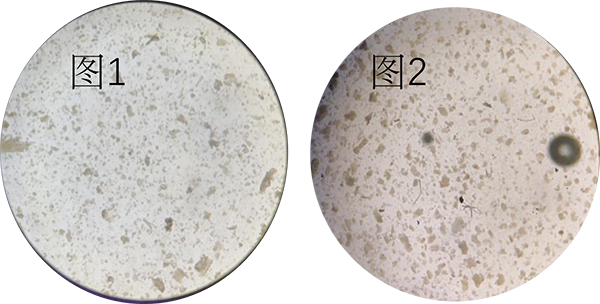
(6) 使用100μm孔径的筛网过滤,收集滤液,于300g富集离心5min后弃去上清,添加原代缓冲液 B再次重悬,300g富集离心5min后弃去上清。(沉淀过少或无红细胞时进入步骤8)
(7) 细胞沉淀含有红细胞,弃上清,加入1-2mL红细胞裂解液1-2min后,稀释至10mL,再次离心(300g离心5min)。
(8) 基质胶计算:第6步后观察收集到的细胞沉淀体积量,添加25倍细胞沉淀体积的基质胶重悬铺板。(可借鉴图2-1,按照如图细胞沉淀量分别加200ul、150ul、100ul、50ul基质胶)

(9) 24孔细胞培养板为例,每孔点25-30ul组织基质胶混合物进行铺板(关键步骤:基质胶维持在0-4℃条件下操作)。
(10) 将铺好的培养板放入37℃培养箱中10-15min,基质胶凝固后,添加500-750ul肠癌类器官培养基A(恢复室温)进行培养。
3、 类器官传代培养(以24孔板为例)
实验材料:(除冰盒外均需无菌)
传代缓冲液G(4℃预冷)、类器官传代消化液D(室温或37℃)、基质胶(提前一晚放入4℃冰箱融化)、肠癌类器官培养基A(室温或37℃)、15mL离心管、24孔板、冰盒
(1) 移液器吸去培养基,每孔添加1-2ml 4℃预冷传代缓冲液G放置2min。
(2) 移液枪轻柔吹打基质胶,收集于15ml离心管中,4℃静置10-15min。(每6-8孔为一组)
(3) :
3.1类器官数量不足或体积较小时: 300g离心5min弃去上清,添加1mL类器官传代培养缓冲液G重悬移入1.5ml离心管,300g离心5min弃去上清进行第4步。
3.2类器官数量较多或体积较大时:300g离心5min弃去上清,可选择机械消化或消化液消化;
1)机械消化:使用1mL枪头吹打20-30次,直至吹打至(图3-图3-1)状态时即可停止;
2)消化液消化(2-4min):加入1-2mL类器官传代消化液D,将细胞沉淀吹散后在室温消化,在显微镜下观察,每隔一分钟吹打一次,直至消化至(图4-图4-1)状态时即可停止。添加3倍类器官消化液体积的传代缓冲液G终止消化,300g离心5min弃去上清,添加适量类器官传代培养缓冲液G重悬移入1.5ml离心管,300g离心5min弃去上清,进行第4步。
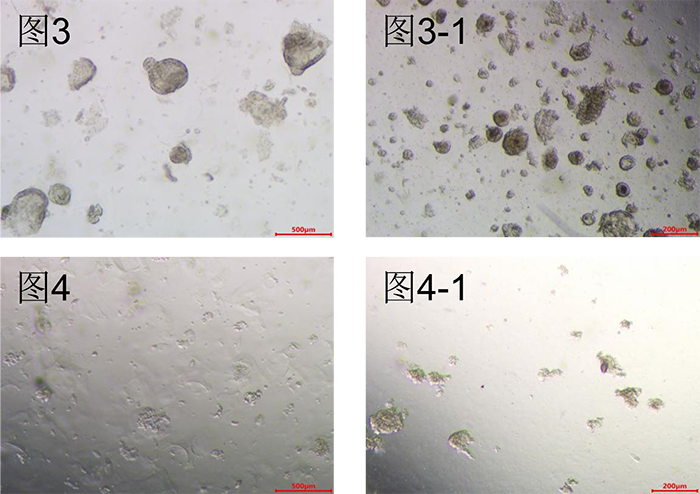
关键步骤:离心后若管底沉淀较少、未见细胞、基质胶未分层等情况,可再次重悬,提高离心力离心一次。
(4) 类器官收集后,添加25倍类器官沉淀体积的基质胶量重悬类器官,可参考图5(根据类器官沉淀量分别添加300ul、150ul、100ul、50ul基质胶)。
关键步骤:注意此过程在0-4℃条件下操作。(注:离心后上清可吸尽或者留细胞沉淀体积的1倍,若沉淀很少建议预留一些上清液加胶),每孔25-30ul细胞基质胶混合物铺在24孔细胞培养板中,放置培养箱10-15min。基质胶凝固后,每孔添加500-750μl肠癌类器官培养基A。

3、类器官冻存(以24孔板为例)
实验材料(除冰盒外均需无菌):传代缓冲液G(4℃预冷)、类器官冻存液F(4℃)、15mL、冰盒、细胞冻存管、程序降温盒、移液枪
(1) 移液器吸去培养基,每孔添加1-2ml 4℃传代缓冲液G放置2min。
(2) 移液抢轻柔吹打基质胶,收集在15ml离心管中,4℃静置10min。(每6-8孔为一组)
(3) 离心5min弃去上清,添加适量传代缓冲液G再次重悬,300g离心5min弃去上清。
(4) 每三个孔加入2mL类器官冻存液F,轻柔吹打混匀,转至细胞冻存管中,每管1mL;
(5) 做好标记信息,放入程序降温盒中,移至-80冰箱中, 48h后,放入液氮罐中保存。或放入4℃冰箱40min后,放入-20℃冰箱中2h,移至-80℃冰箱中,48h后,放入液氮罐中保存。
4、类器官复苏(以24孔板为例)
实验材料(除冰盒外均需无菌):传代缓冲液G、肠癌类器官培养基A、基质胶、24孔板、冰盒、15mL离心管、水浴锅、3mL巴氏吸管/移液枪
(1) 取10ml传代缓冲液G于15ml离心管中
(2) 从液氮罐中取出冻存的类器官细胞,快速置于 37℃水浴锅中融解。
(3) 水浴融解过程中,需轻轻摇动冻存管,以确保冻存液在短时间内完全融解。
(4) 将解冻后的类器官细胞快速转移至15ml 离心管,使用移液管轻柔吹打6-8次,300g 离心 5分钟,弃上清,收集类器官细胞沉淀。添加适量传代缓冲液G重悬,移入1.5ml离心管300g离心5min,弃上清。
(5) 按每管冻存管添加100ul基质胶重悬,每孔25μl基质胶铺在24孔细胞培养板中,放置培养箱中10-15min成胶,添加500-750μl肠癌类器官培养基A。
5、基质胶使用
在2 - 8℃下基质胶过夜解冻,当使用基质胶时,请将其放在冰盒以防止过早凝固。基质胶在37℃下可在20分钟内形成凝胶。
特点:
4℃连续14天仍可保持较好的流动性
放入37℃培养箱中10-15min即可凝固
培养过程中不易破损,去胶干净不粘培养板。
运用范围:
FOR LABORATORY RESEARCH USE ONLY. NOT FOR USE IN DIAGNOSTIC PROCEDURES
