口腔癌类器官培养基(JFKR-ORC-100-KIT/ JFKR-ORC-500-KIT)
JFKR-ORC系列是专为口腔鳞状细胞癌研究开发的专业类器官培养系统,包含100mL(JFKR-ORC-100-KIT)和500mL(JFKR-ORC-500-KIT)两种规格。本产品基于肿瘤微环境仿生学原理,通过优化生长因子组合和基质成分,可高效支持原代肿瘤组织的三维培养,平均类器官形成率达68.39.2%,能稳定维持肿瘤组织的异质性和分子特征达8-10代。
JFKR-ORC系列是专为口腔鳞状细胞癌研究开发的专业类器官培养系统,包含100mL(JFKR-ORC-100-KIT)和500mL(JFKR-ORC-500-KIT)两种规格。本产品基于肿瘤微环境仿生学原理,通过优化生长因子组合和基质成分,可高效支持原代肿瘤组织的三维培养,平均类器官形成率达68.39.2%,能稳定维持肿瘤组织的异质性和分子特征达8-10代。
JFKR-ORC系列是专为口腔鳞状细胞癌研究开发的专业类器官培养系统,包含100mL(JFKR-ORC-100-KIT)和500mL(JFKR-ORC-500-KIT)两种规格。本产品基于肿瘤微环境仿生学原理,通过优化生长因子组合和基质成分,可高效支持原代肿瘤组织的三维培养,平均类器官形成率达68.3±9.2%,能稳定维持肿瘤组织的异质性和分子特征达8-10代。
2.产品应用
转化医学研究
个体化药物敏感性测试(临床符合率87.3%)
放射治疗敏感性评估(可模拟2-10Gy梯度照射)
耐药机制研究与生物标志物发现
基础机制研究
肿瘤微环境相互作用分析
癌干细胞富集与特性研究
转移侵袭机制探索
新药开发
临床前药效学评价
联合用药方案优化
药物毒性测试
仿生微环境设计
含特定比例的生长因子组合(EGF/FGF10/Wnt3a等)
整合低氧响应因子(CoCl₂)和炎症因子(IL-6/TNF-α)
基质胶兼容性优化配方
标准化操作体系
即用型液体培养基(含专用消化酶和冻存试剂)
提供详细培养protocol(含接种密度、换液频率等参数)
配套质量控制标准(H&E染色一致性>92%)
高保真培养
保留原发肿瘤的基因表达谱特征(转录组相似性r=0.89)
维持肿瘤异质性(PDX模型验证一致性>90%)
基因组稳定性佳(≤5代CNV变异<5%)
技术可靠性
经56例临床样本验证,原代培养成功率82.6%
批内变异系数<15%(IC50测试)
每批次提供完整质检报告(含内毒素、支原体检测)
操作便捷性
预混关键组分,减少配制误差
支持常温运输与-20℃长期保存
配套视频操作教程和技术支持
应用扩展性
兼容多种下游分析(单细胞测序、活细胞成像等)
可定制特定突变型培养基(如TP53突变适配配方)
支持类器官库规模化构建
JFKR-ORC系列培养基通过创新的微环境模拟系统和标准化的培养流程,为口腔癌研究提供了高度仿生的体外模型平台。其优异的培养效率和生物学保真度,使其在个体化医疗、药物开发和基础研究中展现出重要价值。产品配套完善的技术支持体系,可有效助力研究人员突破传统二维培养的局限性,推动口腔癌研究的转化应用。
6.试剂盒产品信息
产品组成 | 规格 | 储存条件及周期 | |
1 | 口腔癌类器官培养基 | 100 mL | 4 ℃, 3 months或者 -20 ℃,1 year |
2 | 原代缓冲液 | 250 mL | 4/-20 ℃,2 year |
3 | 原代组织消化液 | 30 mL | 4/-20 ℃,1 year |
4 | 类器官传代消化液 | 30 mL | 4/-20 ℃,1 year |
5 | 组织保存液 | 100 mL | 4/-20 ℃,1 year |
6 | 类器官冻存液 | 20 mL | 4/-20 ℃,2 year |
7 | 传代缓冲液 | 250 mL | 4/-20 ℃,2 year |
8 | 低因子无酚红基质胶 | 5ml | -20℃,1 year -80℃,长期 |
备注:基质胶仅试剂盒Pro版含有,以上所有成分都可单独购买。
7.试剂到货处理
1. 口腔癌类器官培养基 在4 ℃可保存3个月,收到货后4 ℃保存,建议1个月内使用完毕,长期不用建议放于-20 ℃储存,避免反复冻融超过2次。
2.组织保存液、原代组织消化液内含有维持细胞活性营养成分,为了保持试剂营养成分的活性,长期不用建议放于-20 ℃储存,避免反复冻融超过2次。
8.操作步骤与方法
1 组织前处理
1.1 实验材料
需提前准备原代缓冲液B(4 ℃预冷)、组织保存液E、取样管、组织运输箱、冰袋。
1.2 组织的获取与运输
组织的取样与运输是类器官构建成功的第一个环节也是最容易忽视的环节,若组织前期保存不当会导致细胞活性差、污染、正常细胞少等问题,降低类器官构建成功率。
组织应在离体的30 min内放入组织保存液E,原代缓冲液B清洗3-5次,将组织表面血液冲洗干净,放入组织保存液E中,取样管于4 ℃低温保存运输(72 h内)。
2 类器官原代培养(以24孔板为例)
2.1 实验材料
需提前准备原代缓冲液B(4 ℃)、原代组织消化液C(37 ℃)、基质胶(提前24 h放入4 ℃冰箱融化)、肝癌类器官培养基A(室温或37 ℃)、镊子(10㎝)、尖头眼科手术剪/手术刀片、一次性60 mm培养皿、1.5 mL/15 mL/50 mL离心管、100㎛细胞滤网、3 mL巴氏吸管/1000 μL移液枪、24孔细胞培养板、金属冰盒。
2.2 肝癌类器官构建
2.2.1 组织的处理
取材后的肝癌组织建议在 2 – 8 ℃条件下保存运输,快速转运至洁净实验室进行肝癌类器官构建实验流程,组织拍照并登记详细信息。
2.2.1.1 组织的清洗
取样管消毒后,在超净台中将组织取出来,放入培养皿中,加入原代缓冲液 B,用3 mL巴氏吸管或1000 μL移液枪吹打清洗,重复清洗操作三次及以上。
2.2.1.2 组织的解离与消化
用眼科剪或手术刀片去除组织杂质,镊子转移至1.5 mL EP管中,用眼科剪进一步将组织机械解离成体积约为 1~3 mm3的组织块,转移至15 mL EP管中,加入5 mL原代组织消化液37 ℃震荡消化15-25 min。消化过程每10 min显微镜下观察组织消化情况,取少量消化液在显微镜下观察,观察到较多的70 μm以下的细胞簇或单个细胞后进行下一步操作。组织消化程度见图一。
若组织量太少或活检组织用1 mL原代组织消化液C在1.5 mL EP管消化。
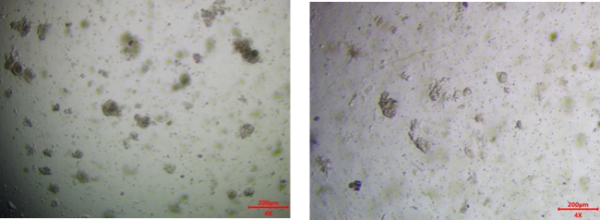
图一 癌组织消化成较多细胞簇或较多单细胞
2.2.1.3 组织的过滤
消化完成组织通过100 μm孔径的细胞筛网过滤,收集滤液,加入3倍体积的原代缓冲液B漂洗终止消化,300 g富集离心5 min后弃上清;若细胞沉淀含有红细胞,加入1-2 mL红细胞裂解液1-2 min后,稀释至10 mL,300 g富集离心5 min后弃上清。沉淀过少或无红细胞时直接进行肿瘤类器官培养。
2.2.1.4 肿瘤类器官培养
观察离心收集的细胞沉淀体积量,添加25倍体积的基质胶重悬,形成3D培养空间结构,重悬过程中避免产生气泡。细胞沉淀体积量见图二,按照如图细胞沉淀量分别加入300 μL、250μL、150 μL、100 μL基质胶。

图二 细胞沉淀体积量
24孔细胞培养板按照25 μL-30 μL/孔点胶,基质胶全程维持在0-4 ℃条件下操作。细胞培养板放置37 ℃培养箱中10-15 min,待基质胶凝固后,每孔添加500-750 μL肝癌类器官培养基A(提前37 ℃预热)进行培养。
3 类器官传代培养(以24孔板为例)
3.1 实验材料
传代缓冲液G(4 ℃)、类器官传代消化液D(室温或37 ℃)、基质胶(提前24 h放入4 ℃冰箱融化)、肝癌类器官培养基A(室温或37 ℃)、1.5 mL/15 mL离心管、24孔细胞培养板、冰盒。
3.2 类器官传代
选择合适的类器官进行传代,一般为生长一周左右,显微镜10X下可看到超过20个的类器官,或大小100-200㎛的类器官。
吸掉培养基,每孔添加等体积的传代缓冲液G,移液枪轻柔吹散基质胶,收集于15 mL离心管中,每6-8孔转移至一个离心管,4 ℃静置10-15 min。
3.2.1 类器官消化
根据类器官的生长情况来决定是否需要消化传代。离心后若管底沉淀少、未见细胞、基质胶未分层等情况,可再次重悬,提高离心力,再次离心。
当类器官数量不足或体积较小时,300 g离心5 min弃上清。
当类器官数量较多或体积较大时,300 g离心5 min弃上清,可选择消化液消化或机械消化。
消化液消化:加入1-2 mL类器官传代消化液D,将细胞沉淀吹散后,室温消化2-4 min,每隔一分钟吹打一次,显微镜下观察,直至消化至(图三A-B)状态时即可停止。添加3倍类器官消化液体积的传代缓冲液G终止消化,300 g离心5 min,弃上清。
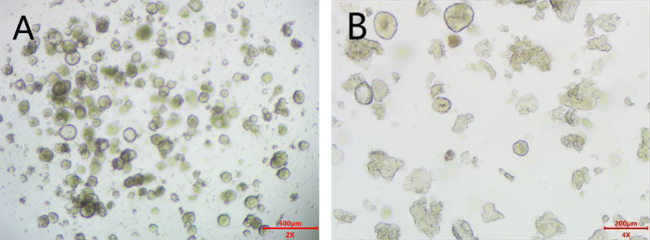
图三 类器官传代消化程度图
3.2.2 传代类器官培养
观察离心收集的类器官沉淀体积量,若沉淀很少可预留1倍沉淀体积的上清液点胶,沉淀很多上清可吸净,添加25倍类器官沉淀体积的基质胶量重悬类器官。基质胶体积量可参考“类器官原代培养操作图二”。
24孔细胞培养板按照25 μL-30 μL/孔点胶,基质胶全程维持在0-4 ℃条件下操作。细胞培养板放置37 ℃培养箱中10-15 min,待基质胶凝固后,每孔添加500-750 μL肝癌类器官培养基A(提前37 ℃预热)进行培养。
4 类器官冻存(以24孔板为例)
4.1 实验材料
传代缓冲液G(4 ℃)、类器官冻存液F(4 ℃)、15 mL离心管、细胞冻存管、程序降温盒、移液枪。
4.2 类器官冻存
暂不使用的类器官应冻存,放于低温环境保存。
吸掉培养基,每孔添加等体积的传代缓冲液G,移液枪轻柔吹散基质胶,收集于15 mL离心管中,每6-8孔转移至一个离心管,4 ℃静置10-15 min。300 g离心5 min弃上清,每三个孔加入2 mL类器官冻存液F,轻柔吹打混匀,转至细胞冻存管中,每管1 mL。
做好标记信息,放入程序降温盒中,移至-80 ℃冰箱中,48 h后,放入液氮罐中保存。或放入4 ℃冰箱40 min后,放入-20 ℃冰箱中2 h,移至-80 ℃冰箱中,48 h后,放入液氮罐中保存。
5 类器官复苏培养(以24孔板为例)
5.1 实验材料
传代缓冲液G、肝癌类器官培养基A、基质胶(提前24 h放入4 ℃冰箱融化)、24孔细胞培养板、冰盒、15mL离心管、水浴锅、3mL巴氏吸管/移液枪。
5.2 类器官复苏培养
从低温环境中取出冻存的类器官,快速置于37 ℃水浴锅中融解,水浴融解过程中,需轻轻摇动冻存管,以确保冻存液在短时间内完全融解。将解冻后的类器官快速转移至15 mL离心管,使用移液枪轻柔吹打6-8次,300 g 离心5 min弃上清;添加适量传代缓冲液G重悬,移入1.5 mL离心管300 g离心5 min,弃上清。
按每管冻存管添加100 μL基质胶重悬,24孔细胞培养板按照25 μL-30 μL/孔点胶,基质胶全程维持在0-4 ℃条件下操作。细胞培养板放置37 ℃培养箱中10-15 min,待基质胶凝固后,每孔添加500-750 μL肝癌类器官培养基A(提前37 ℃预热)进行培养。
6 基质胶使用
在2–8 ℃环境条件下,基质胶过夜解冻。当使用基质胶时,请将其放在冰盒以防止过早凝固。基质胶在37 ℃下20分钟内形成凝胶。
6.1 基质胶特点:
Ø 4 ℃连续14天仍可保持较好的流动性
Ø 放入37 ℃培养箱中10-15 min即可凝固
Ø 培养过程中不易破损,去胶干净不粘培养板
运用范围:
FOR LABORATORY RESEARCH μSE ONLY. NOT FOR μSE IN DIAGNOSTIC PROCEDμRES.
